Etiologia, classificação, imagem clínica, diagnóstico e tratamento da leucemia mielóide aguda.
Contente
 Leucemia afiada — Grupo heterogêneo de clonal
Leucemia afiada — Grupo heterogêneo de clonalDoenças do tumor do tecido hematopoiético caracterizadas descontroladas
proliferação, interrupção da diferenciação e acumulação na medula óssea e
sangue periférico de células hematopoiéticas imaturas.
A leucemia aguda é de 2-3% de tumores malignos
homem. A incidência de leucemia afiada é uma média de 3-5 casos em
100.000 habitantes. Em 75% dos casos, a doença é diagnosticada em adultos, 25%
Casos — em crianças. A proporção média de leucemia afiada mielóide e linfóide
é 6: 1. Em pacientes adultos com idade superior a 40 anos de 80% dos casos
apresentado por formas mielóides, em crianças — 80-90% — linfóide. Mediana
Pacientes com idade com leucemia aguda não-mlublástica — 60-65 anos de idade, afiada
leucemia linfoblástica — 10 anos.
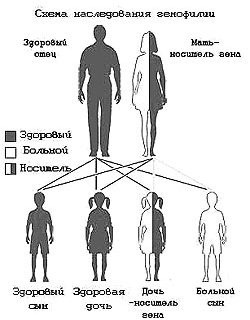
Há uma probabilidade genética de desenvolver aguda
Leukoza mieloide. Há um grande número de relatórios de casos familiares
Doenças, a probabilidade de um IML para os parentes mais próximos do paciente
três acima. Um número de estados inatos pode
aumentar a probabilidade de oml. Na maioria das vezes é a síndrome de Down, na qual a probabilidade de um IML é levantada em
10 — 18 vezes.
Alguns carcinógenos
(causando agentes de tumores) podem ser considerados fatores etiológicos
Oml, como gasolina, tabaco de fumar e radiação ionizante. Mais importante
Fator de risco é superior a 65 anos.
A influência do indivíduo
As características genéticas do corpo, bem como o impacto no corpo de exógeno
Fatores se manifesta no desenvolvimento da leucemia mielóide aguda secundária,
componentes de 5-20% de todos os casos de IML. Em particular, o IML pode desenvolver
Pessoas anteriormente passando por tratamento com vários modos de quimioterapia
Outras formações malignas.
A presença da fase precedente em
a forma de síndrome myelodsplastic (MDS) mais comum em idosos
pacientes também é um importante fator de risco oml. Antitumoriano
Efeitos quimioterápicos, especialmente drogas alquilantes, antraciklines
e epipodofillexinas, aumenta a probabilidade do desenvolvimento do
MDS OML / SECUNDÁRIO. A maior probabilidade da doença cai por 3-5 anos
Após quimioterapia. A aplicação combinada de terapia de quimioterapia / radiação também é significativamente
Aumenta o risco de MDS secundário secundário. Deve-se notar que secundário
Leucemia / MDS surge em todos os pacientes que recebem antitumor
tratamento.
Leucemia aguda é
Consequentemente de dano — Mutações — No material genético do clone
Célula de Hooping. Como resultado, o nível molecular ocorre
Eventos que levam a uma violação do controle sobre o ciclo celular, alterar
Processos de transcrição e produtos de vários reguladores de proteínas-chave. Maligno
Meloloblastos projetam células com oml,
incapaz de amadurecer e diferenciação como resultado de comprometimento
controle genético e acumulação
na medula óssea. Células Lakeclone
interferir com as atividades das células normais, empurrando-as da medula óssea.
Atualmente todos os afiados
Leucemia é tomada para dividir em mielóide e leucemia linfoblástica afiada.
A classificação da leucemia mielóide afiada da OMS é apresentada abaixo.
Classificação da leucemia mielóide afiada
| Nome subespécies | Descrição |
|
Oml S Mudanças genéticas características |
Em pacientes com tais subespécies do IML Geralmente altos níveis de remissão e a previsão é melhor comparativamente com a OML dos outros subespécies. |
|
Oml com displasia Vários Rostkov |
Esta subespécie Inclui pacientes com síndrome mielodsplastica precedente (MDS) ou doença mieloproliferativa (MPB), que vão para o IML. Esta subespécie do IML é mais comum em idosos e Difere perspectiva desfavorável. |
|
Oml i MDS associados ao tratamento anterior |
Esta subespécie OML inclui pacientes que recebem química e / ou tratamento de radiação após que veio o IML ou MDS. Com estas leucemia, pode haver característica Mudanças nos cromossomos, a previsão para eles é muitas vezes pior. |
|
Oml, n Sujeito aos sinais de subespécies listadas |
Inclui Subespécies de oml que não estão incluídas naqueles listados acima. |
Franco-american-british
classificação
Classificação Franco-American-Britânica (Fab)
O sistema compartilha uma IML a 8 subespécies, de M0 por m7, com base nos tipos
células — predecessores de leucócitos, e sobre o grau de maturidade do alterado
células. Determinação de células malignas são realizadas com base
sinais externos com microscopia leve e / ou citogeneticamente, detectando
desvios subjacentes de mudanças nos cromossomos. Diferentes subespécies do IML
Diferente previsão e resposta ao tratamento. Apesar das vantagens da classificação da OMS,
O sistema Fab ainda é amplamente utilizado. Por fab há oito subtipos
Oml.
| Subespécies | Nome | Mudanças Citogenetic |
| M0 |
Minimamente diferenciado Leucemia myeloblástica aguda |
|
| M1 |
Apimentado Leucemia myeloblastic sem amadurecimento |
|
| M2 |
Apimentado Leucemia myeloblástico com amadurecimento de granulócitos |
T (8; 21) (Q22; Q22), t (6; 9) |
| M3 |
Promelocyrtar, Ou promelocyrtar agudo leucemia (pavimento op) |
t (15; 17) |
| M4 | Apimentado Leucemia mielomocítica |
INV (16) (p13q22), Del (16q) |
| M4eo |
Myelonocal Combinado com eosinofilia de medula óssea |
INV (16), T (16; 16) |
| M5 |
Monoblástico agudo leucemia (m5a) ou aguda Leucemia monocystary (M5B) (M5B) |
Del (11q), t (9; 11), t (11; 19) |
| M6 |
Eritiloide picante leucemia, incluindo leucemia eritrocitária (M6a) e muito raro limpo Leucemia eritiloide (M6b) |
|
| M7 |
Apimentado Leucemia megakariloblástica |
T (1; 22) |
| M8 |
Basofílico agudo leucemia |
Quadro clínico
A imagem clínica da leucemia aguda é determinada pela gravidade
Síndromes Básicas:
-
Anêmico — reduziu os níveis de hemoglobina e
o número de eritrócitos, que se manifesta
Fraqueza, diminuição da capacidade de trabalho, sonolência, manifestações
insuficiência cardíaca, batimento cardíaco,
fraqueza, falta de ar, palidez de pele e membranas mucosas, ortostáticas
hipotensão, angina secundária e infarto do miocárdio, inteligente
Chromota, clínica de insuficiência respiratória em pacientes com crônica
Doenças broncho-pulmonares (DPOC). -
Granulocitoopenic — Complicações infecciosas,
devido a uma diminuição no número de granulócitos no sangue, que é manifestado por alta temperatura e intoxicação, bem como
Clínica local (distritos necróticos, estomatite ulcerativa, osteomielite
Mandíbulas após a extração do dente) ou generalizada (sepse, endocardite infecciosa),
mais frequentemente bacteriana, infecção. -
Hemorrágico
— Hemorragia na pele e hemorragia mucosa, nasal e goma,
Sangramento gastrointestinal e renal, sangramento uterino, elevado
Facção sanguínea durante intervenções operacionais. -
Proliferativo
— Linfadenopatia, esplenomegalia, hepatomegalia, gengivite hiperplásica,
Dores nos ossos, distúrbios da função dos nervos do cérebro craniano, dor de cabeça, violações
visão, general e focal neurológico
sintomatismo, dor de cabeça, priapismo. -
Inxicação
— Fraqueza, declínio no apetite, perda de peso, suor.
Diagnóstico de leucemia afiada
 Primeiro
Primeiro
Passo no diagnóstico é
Análise clínica do sangue, tomando amostra de sangue das veias. Na amostra de sangue
O número de glóbulos (eritrócitos, leucócitos e seus subtipos é determinado, e
Também plaquetas). Quando a descoberta na análise clínica do sangue mais de 20%
As células blastos podem ser diagnosticadas com leucemia aguda.- No
a ausência de sangue suficiente para diagnosticar o número de explosões, bem como
O objetivo da verificação precisa do diagnóstico usando métodos adicionais
Estudos são mostrados para realizar uma biópsia de aspiração da medula óssea.
O estudo da medula óssea inclui um estudo de aspiração de medula óssea
(Análise do meu exame citológico do celular), em casos raros, a gases de gastos é realizada
medula óssea para um estudo histológico da medula óssea. - EM
Qualidade de métodos de pesquisa adicionais para determinar a variante de
Leucemia e marcadores prognósticos são realizados:
-
Cytooquímico
Pesquisa (mieloferixidase, eserase, glicogênio) -
Citogenetic
estude — detecção de anomalias cromossômicas, como ausentes ou
Cromossomos adicionais nas células da medula óssea por análise padrão
Metafaz ou método de peixe
(Fluorescente
Em. Hibridização
situ — Método baseado na habilidade
DNA cromossômico (alvo) para contatar sob certas condições com
Sequências de DNA (sondas), complementar este DNA cromossômico. No
A adesão à sonda de substância fluorescente produz análise de DNA por sua
Localização das células em células interfase). Os resultados da citogenética
Estudos são usados tanto a importância diagnóstica quanto o prognóstico.
| Êxodo | Desvios | Sobrevivência de 5 anos | Frequência recúdica |
| Favorável |
T (8; 21), T (15; 17), INV (16) |
70% | 33% |
| Satisfatório |
Não Revelado, +8, +21, +22, Del (7q), Del (9T), violações 11T23, todos os outros Mudanças estruturais ou numéricas |
48% | cinquenta % |
-
Biológico molecular
pesquisa (pesquisa genética é realizada para identificar características
mutações que podem afetar o resultado da doença — Por exemplo, FLT3-tirosina quinase, gene CD117, aposentado para a síntese do receptor
Kit de fator de crescimento de células-tronco, genes da cebola,
Baalc, ERG, NPM1. -
Estude
Em células tumorais de antígenos diferenciais (CD) por citometria de fluxo (imunofenotipagem).
No futuro em pacientes com afiada
leucemia reescentual da medula óssea, a fim de
Determinar o efeito da terapia, a integralidade da remissão alcançada e a fase de processo
(remissão, estabilização, progressão).
Estágios clínicos e fases da doença
-
Primário-ativo
estágio — Intervalo de tempo entre as primeiras manifestações clínicas
Doenças, diagnóstico e primeira remissão completa -
Cheio
Remissão hematológica clínica — O número de células de explosão no mielograma
Diminui menos de 5%, não há focos extra-vistos leucêmicos
lesões, enquanto no sangue periférico não devem ser jorrantes,
Número de plaquetas 100×109 / l leukocytes 2,5 x
109 / L, granulócitos 1,0 x
109 / L, nível de hemoglobina de 100 g / l.
Recentemente, o conceito de biológica citogenética e molecular
remissão. -
Estágio
doença mínima residual (residual). -
Recurador
Doenças (medula óssea, surto extraótico). -
terminal
estágio.
Tratamento
Antes de começar o tratamento, uma completa clínica
Exame do paciente para avaliar o estado de patologia concomitante
Sistemas cardiovasculares, respiratórios, urogenitais, sistema nervoso central.
Inclui um teste de sangue bioquímico completo, coagulograma, exame em
Hepatite B e C, HIV, vírus do grupo herpes. Ultra-som dos órgãos
Cavidade abdominal, estudo de radiografia de tórax / computador
Tomografia do peito, ECH / ECHO cardiography, CT / MRI HEAD, inspeção
Neurologista, oculista e t.D. Tudo isso é necessário para a escolha certa de tratamento e
Impedindo complicações.
Métodos de tratamento
Pacientes com IML dependem do tipo de doença, fatores prognósticos, idade
o paciente, bem como a patologia relacionada e pode ser dividida em
Métodos terapêuticos potencialmente curativos e terapia de apoio.
Apoiando I
Terapia sintomática
Fundação
O tratamento da OML é terapia de apoio, que inclui o tratamento de infecções intercorrentes, úricultural
diátese, terapia de substituição com componentes de sangue, bem como tratamento
Patologia concomitante.
Baseado em
Therapia de apoio de pacientes com MDS Mentiras Terapia de Substituição
Componentes de sangue. Pacientes com baixo risco de desenvolvimento de anemia OML pode ser
Principal clínico problema significativo. Terapia de reposição
facilita os sintomas da anemia e, portanto, é um tratamento importante.
Frequência
transfusões depende do estado do paciente, a gravidade da anemia, bem como
patologia concomitante, especialmente a necessidade de componentes transbordantes
sangue ao desenvolver no sangramento paciente. O resultado da terapia de substituição
é um aumento no nível de hemoglobina, que estudos mostram,
tem uma correlação positiva com um indicador de qualidade de qualidade.
Transfusão
massa plaquetária é realizada nos casos em que o número de plaquetas
extremamente baixo e / ou há sangramento perigoso. Em desenvolvimento
Coagulopatia (violações no sistema de coagulação sanguínea, por exemplo, redução de nível
Fatores complexos de fibrinogênio ou protrombina) Realização de reforço
Terapia de componentes de plasma de sangue ou
Prepartações recombinantes (Novosvlen, Promroboder e PR.)
Métodos terapêuticos potencialmente curativos
-
 Para controlar os sintomas da doença ou cura do IML em pacientes jovens
Para controlar os sintomas da doença ou cura do IML em pacientes jovens
Quimioterapia intensiva para destruir o clone de patológico
células e alcançar uma longa remissão. Este método de tratamento
Efeitos colaterais significativos, como a perda de cabelo, a aparência de estomatite
cavidade oral, náusea, vômito, aparência de fezes líquidas. Além desses lados
fenômenos, a quimioterapia tem efeitos adversos e saudável
células que exigem uma longa estadia em hematológica
Departamentos. Neste momento, o paciente é realizado sobre células sobre o sangue e
massa de trombócitos, drogas antibacterianas são prescritas para combater
infecção. Se a quimioterapia de indução proporciona controle adequado sobre
células patológicas (estado de remissão), depois restauração do normal
As células do sangue devem começar dentro de algumas semanas. No entanto, mesmo nos casos
Doença de tratamento bem sucedida pode ser devolvida — recurar. - O único
Método conhecido de tratamento capaz de curar a maioria dos pacientes com oml,
é o transplante de haste hematopoiética alogênica (doador)
células. Deve-se ter em mente que este é um procedimento complexo relacionado ao risco
complicações precoces e atrasadas. O resultado do tratamento depende do grau de compatibilidade (compatibilidade HLA) do doador e do paciente
(destinatário), bem como sobre a disponibilidade de células doadores adequadas (disponibilidade
Irmãos de sangue compatíveis e / ou irmãs, disponibilidade do banco doador). Desse modo
O caminho há testemunhos rigorosos e contra-indicações para este tipo de tratamento:
É adequado para os casos em que os pacientes são capazes de transferir
Transplante de células-tronco e ter um doador adequado e atendido tratamento quimioterápico. - Estude
Os mecanismos de desenvolvimento de MDS / Secundário IML, realizados nos últimos anos,
que para esta patologia é caracterizada pela hipermetilização da região do promotor
alguns genes-oncosuppressores, que levam a «silêncio» Estes genes I
Proliferação de células tumorais e transformações no IML. Com base nesse conhecimento
Os chamados agentes hipometais que contribuem foram desenvolvidos
Hipometrtilação de DNA, causando expressão anteriormente «Desabilitado» Genov.
Em maio de 2004, a gestão
EUA para controle de alimentos e drogas (Administração de alimentos e drogas, FDA) emitiu permissão para usar
Preparação de injeção Azacytidin (Vaidaza) para o tratamento de todos os tipos de MDS. Na Federação Russa
A droga foi aprovada para uso em 2010, inclusive para o tratamento de ambos os MDS e IML. Os resultados do estudo mostraram que
A azeticidade prolonga de forma confiável a vida a pacientes com leucemia mielóide aguda,
Transplante de células-tronco programadas / intensivo
quimioterapia. Os estudos mostram que a taxa de sobrevivência de pacientes com um oml sem tratamento moderno é 1,6
meses, enquanto a azeticidade aumenta a vida útil com o IML
11,1 meses, possuindo favorável
Perfil de segurança. além do mais,
a droga, com qualificações suficientes de pessoal médico, pode
Aplicar ambulator.
De acordo com os protocolos adotados na Rússia, o tratamento de pacientes iml, que não são
Adequado para intensivo
A quimioterapia e oml secundária são realizadas por doses baixas de citarabina e / ou com
Usando a terapia de suporte [1]. Tal terapia
Melhora a qualidade de vida dos pacientes, mas não aumenta sua vida
Em comparação com o curso natural da doença. Durante o uso
Azacitidina nesta categoria de pacientes pode mudar radicalmente o fluxo
Doenças (Tabela 1).
tabela
1. A sobrevida total média dos pacientes da IML, dependendo da terapia (indireta
Dados comparativos).
| Sem tratamento | Terapia de apoio | Doses baixas de cytarabin | Azacytidin | |
|
Oml, incluindo número Oml S O número de explosões no mielograma 20-30% |
1,6 | 13,4 | 17.0 | 24.5 |
Sobrevivência mediana de pacientes com IML (20-30% das explosões),
Receber Azacytidine, aumenta para 24,5 meses. Ao mesmo tempo, as diferenças no grupo
Azacytidina com grupos de terapia de apoio e baixas doses de cytarabin
estatisticamente confiável (p = 0,045), independentemente da idade ou cariótipo, e
Meses opcionais de vida são 11,1 e 7,5 respectivamente (mediana
sobrevivência no grupo de terapia de apoio é igual a 13,4 e no grupo baixo
Doses de cytarabin — 17,0 meses) (análise de pesquisa de dados III Fase Aza-001) [2]. Após 2 anos, 50,8% dos pacientes do grupo estavam vivos
Azacitidina, que é 2 vezes mais do que em grupos de comparação (26,2%). Para
Comparação — Pacientes com um oml que não recebem terapia moderna (natural
O curso da doença) morrem dentro de 7 semanas do diagnóstico.
 Para pacientes com um IML, não
Para pacientes com um IML, não
Chemoterapia intensiva / transplante de células-tronco, tratamento
A azetacina pode ser o único meio de prolongamento de vida e
Ajudando a alcançar longa remissão. No estudo da AZA-001 no grupo de azacitidina à resposta da terapia
(Critérios IWG
2000) atingiu 29% dos pacientes (resposta completa e parcial), 49% — alcançou
Melhoria hematológica. Diferenças com grupos de comparação («Suportado
terapia», «Doses baixas de cytarabin») Estatisticamente confiável (5 e 12%, 31 e 25%
respectivamente). O tempo para a progressão da doença foi de 14,1 meses em
Grupo «Azacytididine» e 8,8 meses em grupos de comparação (p = 0,047). Duração
A resposta hematológica foi de 13,6 meses na Azacytidina em comparação com
5,2 meses em terapia tradicionalmente usada (p = 0,002).
Em pacientes com MDS e IML que receberam
Terapia a ascitidina foi observada uma maior probabilidade de independência de
Transfusões da massa eritrócitos: 45% dos pacientes tornaram-se independentes de
Hemotransfono, enquanto em modos tradicionais — Apenas 11% (p < 0.0001).
Assim, o tratamento da ascitidina dos pacientes OML (20-30% das explosões)
acompanhado não só por uma maior expectativa de vida e total
Frequência remissária em comparação com a terapia de apoio e baixas doses de cytarabina,
mas também melhoria hematológica maior e independência
Transfusões. Pacientes com MDS Alto Risco AzacyTidine Therapy
acompanhado de um aumento no tempo antes da transformação em um OML (17,8 meses vs 11,5 meses, p<0,001).
A azeticina está incluída nos protocolos internacionais para tratamento
Pacientes com síndrome myelodsplastic e IML em pacientes com mais de 60 anos.
EUA: No Guia Nacional de Tratamento da OML
Rede oncológica (Nacional Câncer Compreensivo Rede, Nccn, EUA) (2010) A Azacytidine é recomendada para aplicação
pacientes com mais de 60 anos que não são candidatos para altamente visíveis
Quimioterapia. Recomendações são dadas com um alto nível de evidência.
PARA
fenômenos indesejáveis de 3-4 graus em desenvolvimento no contexto do tratamento da azeticidade,
Tratar hematologic (71.4%), incluindo trombocitopenia (85%), neutropenia
(91%) e anemia (5